

*31% mindre försämring av kognitiva symtom och funktioner under 18 månader hos lecanemab-behandlade patienter jämfört med placebogruppen (genomsnittlig förändring från baslinjen enligt CDR-SB 1,22 jämfört med 1,75; gruppskillnad −0,535; 95% KI −0,778; −0,293).
LÅT PATIENTERNA STANNA LÄNGRE I ETT TIDIGARE STADIUM AV SJUKDOMEN GENOM TIDIG OCH KONTINUERLIG BEHANDLING MED LEQEMBI®
Mer tid i ett lindrigare sjukdomsstadium
- Patienter som fick LEQEMBI stannade i ett lindrigare sjukdomsstadium längre*, mätt med CDR-SB (kognitiv och funktionell bedömningsskala) jämfört med placebo
Effekten ökar med tiden
- Effekten av LEQEMBI-behandling ökar med tiden
Resultaten är konsekvent statistiskt signifikanta över alla huvudsakliga effektmått
- LEQEMBI-behandlingen ledde till konsekvent långsammare sjukdomsprogression även visat med ADAS-Cog14 och ADCS-MCI-ADL, samt en rensning av amyloid-β (amyloid-PET), var och en med statistisk signifikans jämfört med placebo

*31% mindre försämring av kognitiva symtom och funktioner under 18 månader hos lecanemab-behandlade patienter jämfört med placebogruppen (genomsnittlig förändring från baslinjen enligt CDR-SB 1,22 jämfört med 1,75; gruppskillnad −0,535; 95% KI −0,778; −0,293).
LEQEMBI – LÅNGSAMMARE PROGRESSION BETYDER MER SJÄLVSTÄNDIG TID
LEQEMBI 10 mg/kg varannan vecka N= 757, jämfört med placebo n= 764, indicerad population.
CDR-SB: 31% inbromsning i försämringen* av kognitiva symtom och funktioner
Mätt under 18 månader, jämfört med placebo hos patienter med Alzheimers sjukdom (AD), mätt med Clinical Dementia Rating Scale (CDR-SB).
*Justerad genomsnittlig förändring från baslinjen på CDR-SB 1,217 jämfört med 1,752; gruppskillnad −0,535; 95% KI (−0,778, −0,293).
- minne
- orienteringsförmåga
- omdöme problemlösningsförmåga
- sociala/allmänna aktiviteter
- hem och fritid
- personlig hygien
ADCS MCI-ADL: 33% mindre försämring° av förmåga att utföra vardagliga uppgifter (ADL)
Mätt under 18 månader, jämfört med placebo hos patienter med AD, mätt med ADC MCI-ADL.
°Justerad genomsnittlig förändring från baslinjen på ADAS MCI-ADL −3,873 jämfört med −5,809; gruppskillnad 1,936; 95% KI (1,029; 2,844).
- betala räkningar
- navigera utanför hemmet, gå och handla
- använda hushållsapparater
- hitta personliga tillhörigheter
- klä på sig
- klara sig ensamma hemma
ADAS-Cog 14: 26% mindre försämring i kognitiv förmåga§
Mätt under 18 månader, jämfört med placebo hos patienter med AD, mätt med ADAS-Cog14.
§Justerad genomsnittlig förändring från baslinjen på ADAS Cog14 4,389 jämfört med 5,901; gruppskillnad −1,512; 95% KI (−2,486; −0,538).
ADAS-Cog:
- ordigenkänning
- fördröjt ordminne
- ordminne
- orientering
ADCS-iADL:
- laga mat
- telefonsamtal
- handla
- komma i tid till vårdbesök och liknande
- vara ensam hemma m.m.
LEQEMBI® – LÅNGSAMMARE PROGRESSION BETYDER MER OBEROENDE TID
LEQEMBI® 10 mg/kg varannan vecka N= 757, jämfört med placebo n= 764, indicerad population.
CDR-SB: 31% inbromsning i försämringen* av kognitiva symtom och funktioner
*Justerad genomsnittlig förändring från baslinjen på CDR-SB 1,217 jämfört med 1,752; gruppskillnad −0,535; 95% KI (−0,778, −0,293).
- minne
- orienteringsförmåga
- omdöme problemlösningsförmåga
- sociala/allmänna aktiviteter
- hem och fritid
- personlig hygien
Under 18 månader, indicerad population, jämfört med placebo hos patienter med Alzheimers sjukdom, mätt med Clinical Dementia Rating Scale (CDR-SB).
ADCS MCI-ADL: 33% mindre försämring° av förmåga att utföra vardagliga uppgifter (ADL), exempelvis:
*Justerad genomsnittlig förändring från baslinjen på ADAS MCI-ADL −3,873 jämfört med −5,809; gruppskillnad 1,936; 95% KI (1,029; 2,844).
- betala räkningar
- navigera utanför hemmet, gå och handla
- använda hushållsapparater
- hitta personliga tillhörigheter
- klä på sig
- klara sig ensamma hemma
Under 18 månader, indicerad population, jämfört med placebo hos patienter med Alzheimers sjukdom, mätt med ADC MCI-ADL.
ADAS-Cog 14: 26% mindre försämring i kognitiv förmåga§
Justerad genomsnittlig förändring från baslinjen på ADAS Cog14 4,389 jämfört med 5,901; gruppskillnad −1,512; 95% KI (−2,486; −0,538).
ADAS-Cog:
- ordigenkänning
- fördröjt ordminne
- ordminne
- orientering
ADCS-iADL:
- laga mat
- telefonsamtal
- handla
- komma i tid till vårdbesök och liknande
- vara ensam hemma m.m.
Under 18 månader, indicerad population, jämfört med placebo hos patienter med Alzheimers sjukdom, mätt med ADAS-Cog14.
RESULTAT FÖR CDR-SB, ADAS-COG14 OCH ADCS MCI-ADL I CLARITY-AD
| Indicerad population | ||
|---|---|---|
| Kliniska effektmått | LEQEMBI 10 mg/kg varannan vecka | Placebo |
| CDR-SB | N=757 | N=764 |
| Genomsnitt vid baslinjen (SD) | 3.18 (1.346) | 3.23 (1.343) |
| Justerad genomsnittlig förändring från baslinjen vid 18 månader, skillnad från placebo (95% KI) | 1.217 -0.535 (-0.778, -0.293) | 1.752 |
| ADAS-Cog14 | N=757 | N=764 |
| Genomsnitt vid baslinjen (SD) | 24.46 (7.081) | 24.40 (7.576) |
| Justerad genomsnittlig förändring från baslinjen vid 18 månader, skillnad från placebo (95% KI) | 4.389 -1.512 (-2.486, -0.538) | 5.901 |
| ADCS MCI-ADL | N=757 | N=764 |
| Genomsnitt vid baslinjen (SD) | 41.15 (6.616) | 40.72 (6.937) |
| Justerad genomsnittlig förändring från baslinjen vid 18 månader, skillnad från placebo (95% KI) | -3.873 1.936 (1.029, 2.844) | -5.809 |
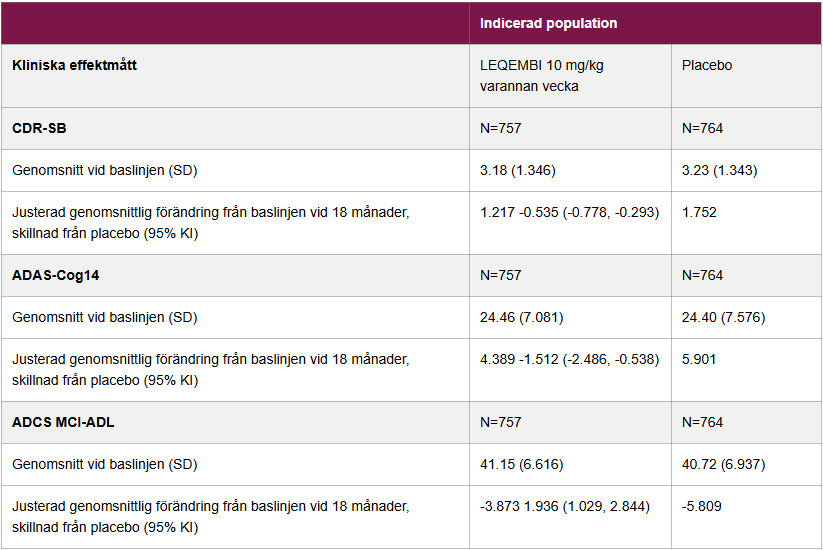
CDR-SB = Clinical Dementia Rating – sum of boxes. ADAS-Cog14 = Alzheimer’s Disease Assessment Scale.° ADAS MCI-ADL = Alzheimer’s Disease Cooperative Study-Activities of Daily Living Scale for Mild Cognitive Impairment.
LEQEMBI HAR UTVÄRDERATS SPECIFIKT FÖR TIDIG ALZHEIMERS SJUKDOM
Effekten av LEQEMBI utvärderades kliniskt i en dubbelblindad, placebokontrollerad, randomiserad studie som omfattade patienter med tidig Alzheimers sjukdom och bekräftad amyloidpatologi:
62% av patienterna hade lindrig kognitiv störning
38% av patienterna befann sig i sjukdomsstadiet med lindrig demens
Det primära effektmåttet var förändring från baslinjen vid 18 månader i CDR-SB.
Över 18 månader, bromsade LEQEMBI försämringen av kognitiva symtom och funktion med 31% jämfört med placebo, mätt med CDR-SB i den indicerade populationen.
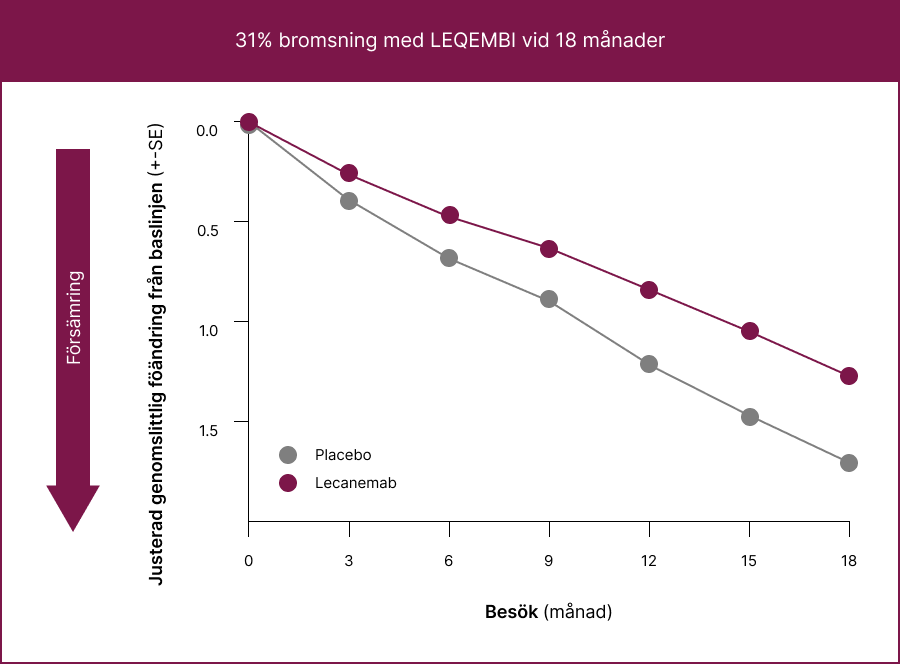
LEQEMBI bromsade signifikant sjukdomsprogressionen med 31% enligt CDR-SB-skalan vid 18 månader och vid alla tidpunkter med början vid 6 månader.1
* CDR-SB = Clinical Dementia Rating – sum of boxes.
SAMTLIGA VIKTIGA SEKUNDÄRA EFFEKTMÅTT
Behandling med LEQEMBI gav långsammare sjukdomsprogression även enligt mätskalorna ADAS-Cog14 och ADCS-MCI-ADL för kognition och funktion, samt rensning av amyloida plack visat med amyloid-PET. Samtliga dessa parametrar visade med statistiskt signifikant skillnad jämfört med placebo hos den indicerade populationen.
ADCS MCI-ADL: 33% mindre försämring° i patienternas förmåga att utföra vardagliga uppgifter (ADL)
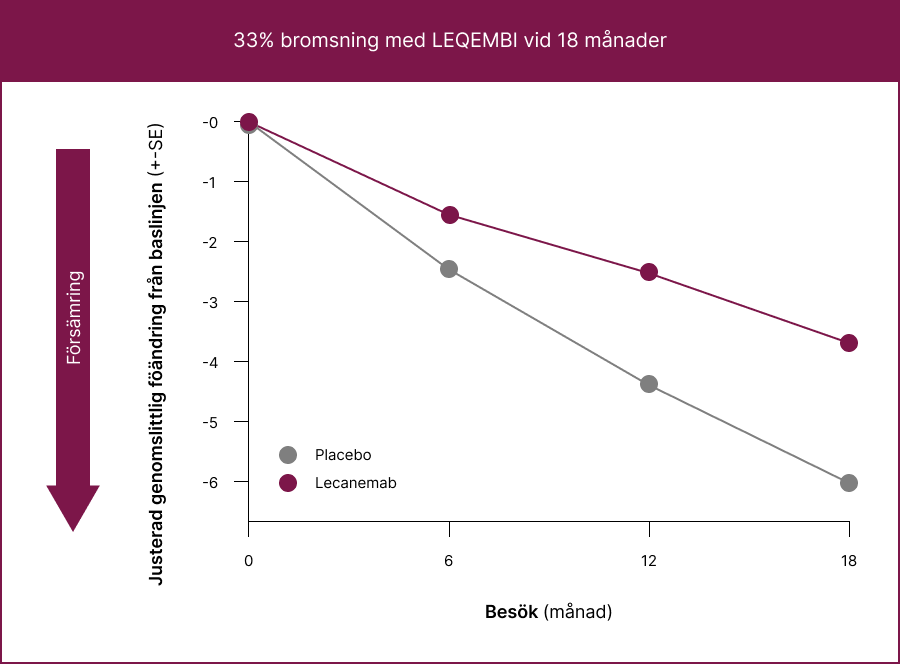
LEQEMBI bromsade signifikant sjukdomsprogressionen enligt ADCS MCI-ADL-skalan med 33% vid 18 månader och vid alla tidpunkter med början vid 6 månader.1
° ADAS MCI-ADL = Alzheimer’s Disease Cooperative Study-Activities of Daily Living Scale for Mild Cognitive Impairment.
ADAS-Cog14 26% mindre försämring§ i kognitiv förmåga
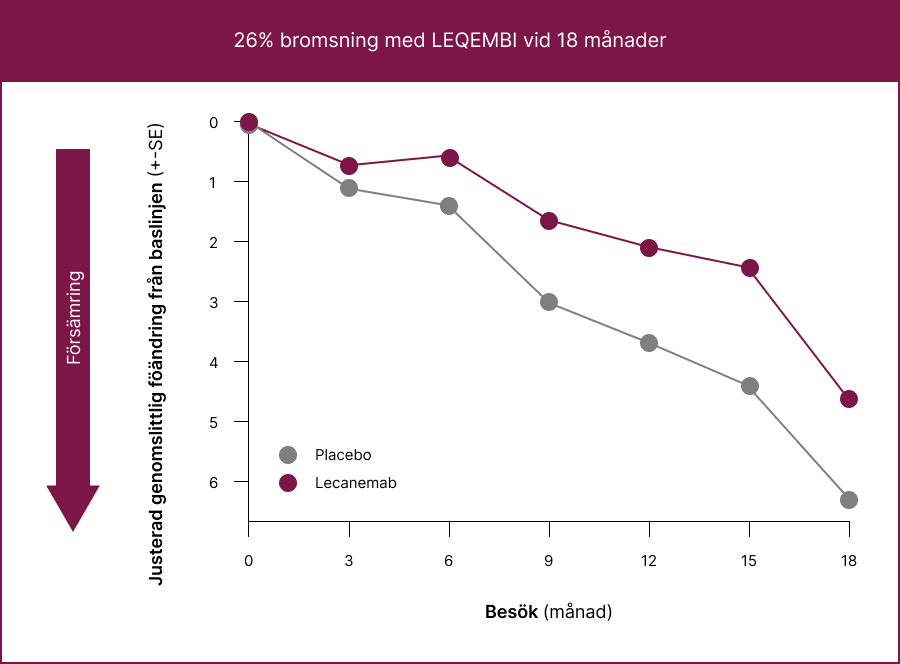
LEQEMBI bromsade signifikant sjukdomsprogressionen enligt ADAS-Cog14-skalan med 26% vid 18 månader och vid alla tidpunkter med början vid 6 månader.1
§ADAS-Cog14 = Alzheimer’s Disease Composite Score.
LEQEMBI rensar effektivt amyloid-β plack
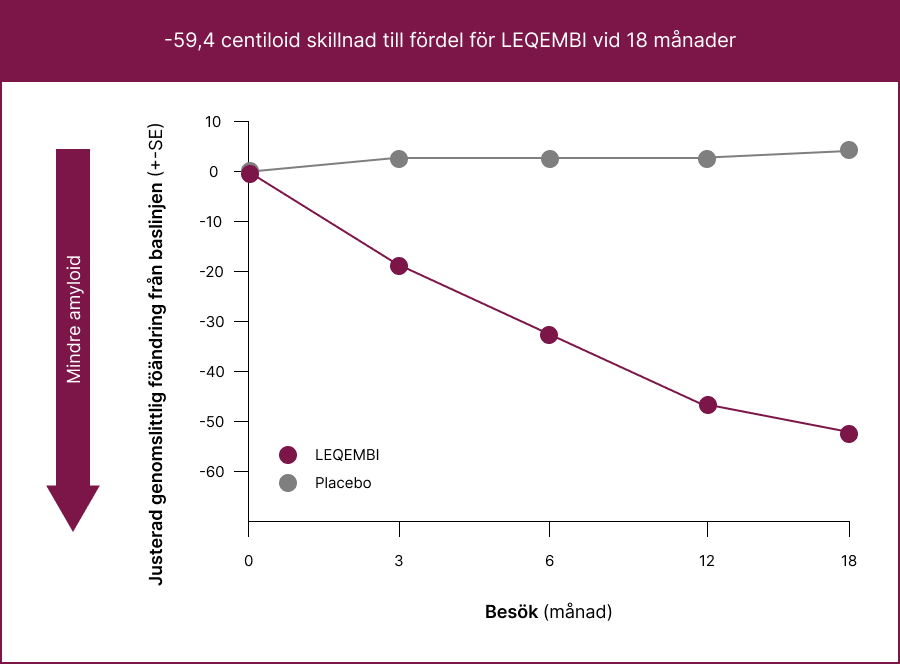
Effekten av LEQEMBI på amyloid beta-placknivåerna i hjärnan utvärderades med hjälp av PET-avbildning med visuell avläsning och kvantifierades med hjälp av metoden Standard Uptake Value Ratio (SUVR) och centiloidskalan. Den genomsnittliga förändringen från baslinjen i förhållande till placebo var statistiskt signifikant för LEQEMBI 10 mg/kg varannan vecka vid vecka 79 hos den indicerade populationen (−59,437).
Referenser
1. van Dyck CH, Swanson CJ, Aisen P, et al. Lecanemab in Early Alzheimer’s Disease. N Engl J Med. 2023;388(1):9−21.
2. LEQEMBI Produktresumé







